Se você já fez um PET scan, sabe que é uma provação. Os exames ajudam os médicos a detectar o cancro e a monitorizar a sua propagação, mas o processo em si é um pesadelo logístico para os pacientes.
Tudo começa com um jejum de quatro a seis horas antes de entrar no hospital – e boa sorte para você se você mora na zona rural e o hospital native não possui um scanner PET. Ao chegar ao hospital, você recebe uma injeção de materials radioativo, após o qual você deve esperar uma hora enquanto ele percorre seu corpo. Em seguida, você entra no scanner PET e tenta ficar imóvel por 30 minutos enquanto os radiologistas adquirem a imagem. Depois disso, você tem que ficar fisicamente longe de idosos, jovens e mulheres grávidas por até 12 horas porque você fica literalmente semi-radioativo.
Outro gargalo? Os scanners PET estão concentrados nas grandes cidades porque os seus traçadores radioactivos devem ser produzidos em cíclotrões próximos – máquinas nucleares compactas – e utilizados em poucas horas, limitando o acesso em hospitais rurais e regionais.
Mas e se você pudesse usar IA para converter tomografias computadorizadas, que são muito mais acessíveis e baratas, em tomografias PET? Essa é a proposta da RADiCAIT, uma spin-out de Oxford que saiu do sigilo este mês com US$ 1,7 milhão em financiamento pré-semente. A startup com sede em Boston, que é finalista do Prime 20 no Startup Battlefield no TechCrunch Disrupt 2025, acaba de abrir uma arrecadação de US$ 5 milhões para avançar em seus testes clínicos.
“O que realmente fazemos é pegar a solução de imagens médicas mais restrita, complexa e cara em radiologia e substituí-la pelo que é mais acessível, simples e acessível, que é a tomografia computadorizada”, disse Sean Walsh, CEO da RADiCAIT, ao TechCrunch.
O ingrediente secreto do RADiCAIT é seu modelo elementary – uma rede neural profunda generativa inventada em 2021 na Universidade de Oxford por uma equipe liderada pelo cofundador e diretor de informações médicas da startup, Regent Lee.
O modelo aprende comparando tomografias computadorizadas e PET, mapeando-as e identificando padrões de como elas se relacionam entre si. Sina Shahandeh, tecnólogo-chefe do RADiCAIT, descreve-o como uma conexão de “fenômenos físicos distintos”, traduzindo a estrutura anatômica em função fisiológica. Em seguida, o modelo é orientado a prestar atenção additional a características ou aspectos específicos dos exames, como certos tipos de tecido ou anormalidades. Esta aprendizagem focada é repetida muitas vezes com muitos exemplos diferentes, para que o modelo possa identificar quais padrões são clinicamente importantes.
Evento Techcrunch
São Francisco
|
27 a 29 de outubro de 2025
A imagem ultimate que vai aos médicos para revisão é criada pela combinação de vários modelos trabalhando juntos. Shahandeh compara a abordagem ao AlphaFold do Google DeepMind, a IA que revolucionou a previsão da estrutura de proteínas: ambos os sistemas aprendem a traduzir um tipo de informação biológica em outro.
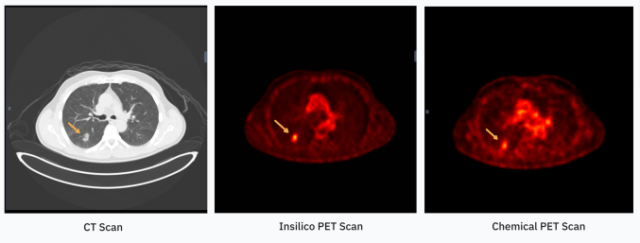
Walsh afirma que a equipe do RADiCAIT pode provar matematicamente que suas imagens PET sintéticas ou geradas são estatisticamente semelhantes aos exames PET químicos reais.
“Isso é o que nossos testes mostram”, disse ele, “que a mesma qualidade de decisão foi tomada quando o médico, radiologista ou oncologista recebe uma PET química ou [our AI-generated PET].”
O RADiCAIT não promete substituir a necessidade de exames PET em ambientes terapêuticos específicos, como a terapia com radioligantes, que mata células cancerígenas. Mas para fins de diagnóstico, estadiamento e monitoramento, a tecnologia do RADiCAIT pode tornar obsoletos os exames PET.

“Por ser um sistema tão limitado, não há oferta suficiente para satisfazer a procura de diagnósticos e teragnósticos”, disse Walsh, referindo-se a uma abordagem médica que combina imagens de diagnóstico (ou seja, PET scans) com terapia direcionada para tratar doenças (ou seja, cancro). “Portanto, o que pretendemos fazer é absorver essa demanda no lado diagnóstico. Os próprios scanners PET devem compensar o lado teragnóstico.”
O RADiCAIT já iniciou pilotos clínicos especificamente para testes de câncer de pulmão com grandes sistemas de saúde como Mass Common Brigham e UCSF Well being. A startup agora está realizando um ensaio clínico da FDA – um processo mais caro e complexo que está impulsionando a rodada inicial de US$ 5 milhões do RADiCAIT. Uma vez aprovado, o próximo passo será fazer pilotos comerciais e demonstrar a viabilidade comercial do produto. O RADiCAIT também deseja executar o mesmo processo – pilotos clínicos, ensaios clínicos, pilotos comerciais – para casos de uso colorretal e de linfoma.
Shahandeh disse que a abordagem do RADiCAIT de usar IA para produzir insights válidos sem o fardo de testes difíceis e caros é “amplamente aplicável”.
“Estamos explorando extensões na radiologia”, acrescentou Shahandeh. “Espere ver inovações semelhantes ligando domínios da ciência dos materiais à biologia, química e física, onde quer que as relações ocultas da natureza possam ser aprendidas.”
Se você quiser saber mais sobre RADiCAIT junte-se a nós no Disrupt, de 27 a 29 de outubro em São Francisco. Saiba mais aqui.